金属与酸之间发生的是置换反应,常用的是活泼的金属单质如锌(Zn)和铁(Fe)镁(Mg)等,酸有盐酸(HCⅠ),硫酸(H2SO4)以及硝酸(HNO3),方程式:Zn十2HCI=ZnCⅠ2+H2↑Zn+H。金属与酸的反应?更多详情请大家跟着小编一起来看看吧!
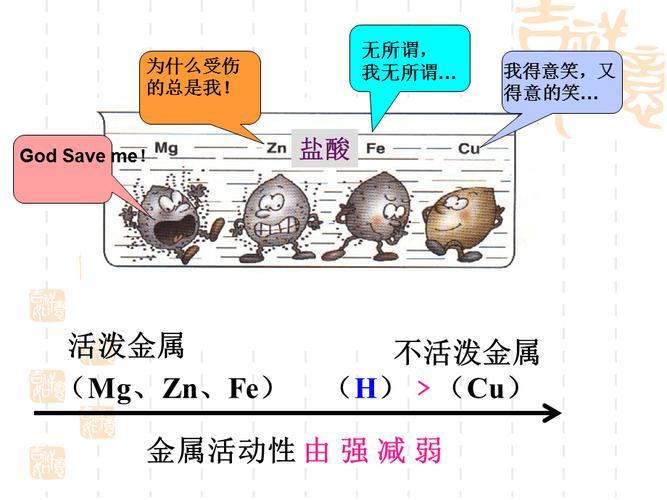
金属与酸的反应(1)
金属与酸之间发生的是置换反应,常用的是活泼的金属单质如锌(Zn)和铁(Fe)镁(Mg)等,酸有盐酸(HCⅠ),硫酸(H2SO4)以及硝酸(HNO3),方程式:
Zn十2HCI=ZnCⅠ2+H2↑
Zn+H2SO4=ZnSO4十H2↑
Zn十2HNO3=Zn(NO3)2十H2↑
Fe十2HCⅠ=FeCl2十H2↑
Fe十H2SO4=FeSO4+H2↑
Fe十2HNO3=Fe(NO3)2十H2↑
Mg十2HCⅠ=MgCⅠ2十H2↑
Mg十H2SO4=MgSO4十H2↑

金属与酸的反应(2)
①排在金属活动性顺序表H前面的金属,和非氧化性酸(如盐酸、稀硫酸等)反应时得到的是H2。例如
Zn+H2SO4===ZnSO4+H2↑。
②排在金属活动性顺序表H前面的金属,和氧化性酸(如稀硝酸、浓硫酸、浓硝酸等)反应时不能得到纯H2。例如Zn+2H2SO4(浓)===ZnSO4+SO2↑+2H2O,但随着反应的进行,由于有水生成,浓硫酸会变稀,因此后期才会有H2产生。
③特殊的两金属Al、Fe在常温下,遇到强氧化性浓硝酸或浓硫酸时,形成极薄的钝化膜,发生钝化现象,保护金属不再和浓硝酸或浓硫酸反应。
④排在金属活动性顺序表H后面的金属(Cu→Ag),不和非氧化性酸反应,遇到强氧化性酸时,发生的是氧化还原反应,例如
Cu+4HNO3(浓)===Cu(NO3)2+2NO↑+2H2O,
3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O。
⑤排在金属活动性顺序表H后面的金属(Pt→Au),不和非氧化性酸反应,遇到强氧化性酸(如稀硝酸、浓硫酸、浓硝酸等)时,一般也不发生氧化还原反应,但是遇到极强的氧化剂[例如王水(硝酸和盐酸的体积比是1:3)]时能发生氧化还原反应,例如
Au+HNO3+3HCl===AuCl3+2H2O+NO↑









